Kan proteiner fra alger give blinde synet tilbage?
At blinde på mirakuløs vis får synet igen, lyder nok mest af alt som en passage fra biblen. Men med ny teknologi og forskning er dette mirakel måske tættere på at blive virkelighed end nogensinde før. En ny teknik kaldet optogenetik kan nemlig gøre nerveceller i stand til at opsamle synsindtryk!
Af Cecilie Vasehus Holck
Forestil dig, at du med en kontakt kan tænde og slukke for de nerveceller, du har i kroppen. Med optogenetik kan du netop det, og her er kontakten noget så simpelt som lys. Optogenetik er en relativt ny metode inden for hjerneforskning, der går ud på at indsætte lysfølsomme proteiner, kaldet opsiner, i nerveceller. Opsiner kommer blandt andet fra alger, og når de bliver belyst med lys med en bestemt bølge længde, kan opsiner frembringe en elektrisk impuls i nervecellerne. Det er netop gennem elektriske impulser og deres samspil med neurotransmittere, at vores nerveceller kommunikerer. Det betyder, at man med optogenetik kan kontrollere kommunikationen mellem nervecellerne – og dét undersøger forskere, om man kan bruge til at genskabe den ødelagte kommunikation mellem øjnene og hjernen hos blinde.
Retinitis pigmentosa – en snigende sygdom
Lysfølsomme nerveceller er i sig selv ikke noget nyt, og vi har dem allerede i kroppen. Det er med dem, vi ser alt fra en smuk solnedgang til en grå leverpostejmad. De lysfølsomme nerveceller er sanseceller, og de er grundstenene i vores synssans. Sansecellerne sidder i vores øjnes nethinde, hvor de registrerer synsindtryk ved hjælp af synspigmenter, der er menneskets egne opsiner. Sansecellerne videresender herefter informationen til vores hjerner gennem elektriske impulser.
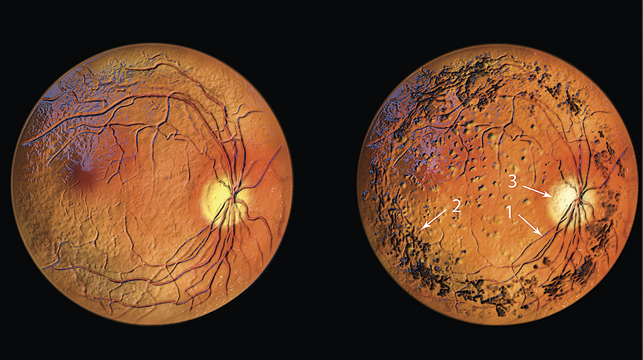
Men hos mange blinde, er sansecellerne blevet nedbrudt eller er uden funktion. Det betyder, at der ikke bliver sendt elektriske signaler fra nethinden til hjernen, og dermed er der ikke nogen synsinformation, hjernen kan bearbejde. Lidelsen kaldes retinitis pigmentosa (RP) og er en arvelig, kronisk sygdom, der rammer ca. 1 ud af 3500. Natteblindhed er ofte det første symptom, og mange opdager ikke sygdommen i starten, da det skarpe syn først forsvinder til sidst. I sidste ende fører sygdommen til hel eller delvis blindhed. På nuværende tidspunkt er der ikke nogen samlet behandling af retinitis pigmentosa.
Sygdommen kan nemlig forårsages af ændringer i omkring 100 forskellige gener i sansecellerne, og én ændring i blot ét af disse gener er nok til at medføre sygdommen. Én samlet behandling er derfor næsten umulig, da sygdommens årsag er forskellig fra patient til patient.
Men med optogenetik kan det umulige måske blive muligt. Nethindens andre nerveceller forbliver nemlig intakte og ved at indsætte nye opsiner i dem, kan man lave kunstige sanseceller. På den måde kan elektriske impulser igen opstå og sendes til hjernen.
Optogenetik – hvordan virker det?
Forsøgsperson får – næsten – synet igen
I 2021 foretog en forskergruppe i et bredt internationalt samarbejde under ledelse af José-Alain Sahel og Botond Roska det første menneskeforsøg nogensinde med optogenetik til behandling af retinitis pigmentosa. Forsøgspersonen var en mand, der havde lidt af sygdommen i mere end 40 år.
Forskerne behandlede forsøgspersonens tilbageværende nerveceller i nethinden med optogenetik. Efter bare 7 måneder, og med lidt hjælp fra lysstimulerende briller, oplevede forsøgspatienten tegn på forøget synsevne. Forskerne foretog også visuelle tests med forsøgspersonen, hvor han udviste en klar forbedring i synsevnen for det behandlede øje.
Opsiner fra grønne alger
Flere opsiner falder i kategorien “channelrhodopsin” – dvs. kanalformede opsiner. Det første channelrhodopsin blev fundet 2002 i grønalgen Chlamydomonas. I naturen bruger alger og bakterier opsiner til navigation og orientering mod sollys. På billedet ses algen Chlamydomanas reinhardtii, hvorfra man fik de to første kanalformede opsiner brugt til optogenetik. Illustration fra: www.rcsb.org
Proteiner fra alger
Opsiner, der bliver brugt til optogenetik, stammer fra alger og bakterier. De er derfor også lidt anderledes end de opsiner, vi mennesker naturligt har i vores sanseceller. Opsiner i mennesker igangsætter en lang række processer inde i cellen, når de bliver udsat for lys. Her er alge-opsiner markant mere ligetil. Alge-opsiner fungerer som en slags dør mellem nervecellens indre og dens omgivelser. Rundt om nervecellen er der forskellige ioner, og når nervecellen bliver belyst, åbnes døren, så ionerne kan strømme ind eller ud ad cellen.
Ionstrømmen forårsager, at den samlede elektriske ladning inde i cellen ændres, og der kan på den måde skabes en elektrisk impuls. Hvor opsiner fra mennesker fungerer som en dørmand, fungerer alge-opsiner i sig selv som en dør. Det betyder også, at man med lys direkte kan åbne og lukke døren. Der findes flere forskellige typer af opsiner, og alt efter typen transporteres enten negative eller positive ioner ind eller ud af cellen. Visse alge-opsiner er endda specifikke til én bestemt ion, for eksempel natrium ioner, der er positivt ladede.
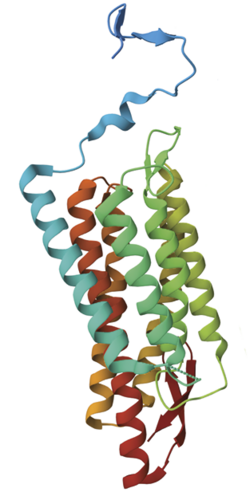
Overordnet består alge-opsiner af syv indbyrdes forbundne spiralformede kæder af aminosyrer, der er proteiners byggesten. Inde i midten af proteinet, er der et stof kaldet retinal, og det er retinal, der er låsen til døren. Når lys rammer retinal, skifter stoffet form, og retinal skubber til de spiralformede kæder. På den måde åbnes døren mellem cellens indre og dens omgivelser. Det vil altså sige, at det er stoffet retinal, som gør opsiner lysfølsomme. Opsiner, vi mennesker naturligt har i sansecellerne, indeholder også retinal.
Virus-postbud bringer opsin ind i cellerne
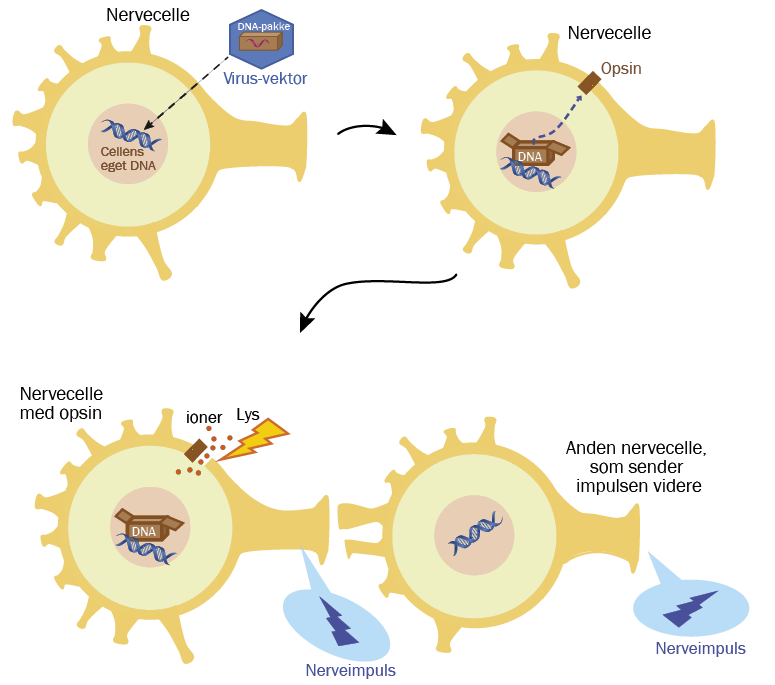
Opsiner indsættes i nerveceller ved hjælp af en virus. Virus har nemlig evnen til at levere gener til andre celler. Ved at pakke opsin-gener i en virus og sende virus ind i nervecellen, kan man indsætte gener, der koder for alge-opsiner i nervecellen. Man skal altså mere se virus som et postbud, der leverer en pakke med gener frem for noget, som giver os feber om vinteren.
Et “virus-postbud” kaldes i fagtermer for en virus-vektor. Man bruger især en virus kaldet adeno-associeret-virus til gen-pakkeleveringen. Den kan ikke sprede sig selv i kroppen og forårsager ikke en ret stor reaktion fra vores immunforsvar. Når opsin-generne er kommet ind i nervecellen, vil nervecellen selv begynde at danne opsiner – gener er nemlig opskriften på proteiner. Dermed vil nervecellen nu kunne reagere på lys, og det betyder, at elektriske impulser kan opstå igen. På den måde kan en normal nervecelle i nethinden forvandles til en kunstig sansecelle.
Stadig udfordringer på vejen
Der er stadig et stykke vej endnu, før optogenetik helt kan hjælpe mennesker med retinitis pigmentosa. En af de største udfordringer er at få de kunstige sanseceller til at kommunikere med resten af nervenetværket på samme måde som naturlige sanse celler. Vores nervesystem er et kæmpe og komplekst netværk, og det kan derfor godt blive en temmelig svær opgave at få løst. Opsin-generne bør derfor helst indsættes i cellelaget lige efter sansecellerne, så størstedelen af det originale netværk genskabes.
Et andet bump på vejen er at finde og udvikle det helt rigtige opsin. Nethinden og øjet kan ikke tåle for stærkt lys, så for at behandlingen kan lykkes, har man brug for et opsin, der ikke kræver meget lys. Dog er der håb forude, og der ses en positiv udvikling i optogenetik som behandlingsmulighed til retinitis pigmentosa.
I juli 2024 modtog Botond Roska og José-Alain Sahel den prestigefyldte Wolf prize indenfor medicin for deres pionerarbejde med optogenetik. Og så sent som i maj 2025 udgav en forskergruppe fra Nanoscope Therapeutics et case study, hvor et nyt syntetisk og forbedret opsin kaldet MCO-010 blev benyttet til behandling af fire personer med retinitis pigmentosa. Forskergruppen rapporterer en klar forbedring i personernes synsevne og formgenkendelse efter behandlingen – endda uden, at lysstimulerende briller var nødvendige.
Optogenetik viser altså fortsat lovende potentiale, og i fremtiden kommer der måske en dag, hvor det umulige bliver muligt, og blinde igen kan få solen at se. ♦
Retinal og A-vitamin

Stoffet retinal er nødvendigt for, at opsiner kan optage lys – både for alge-opsiner og opsiner hos mennesker. Retinal får vi gennem A-vitamin. Gulerødder indeholder store mængder A-vitamin, og grøntsagen er derfor supergod for vores øjne. Foto: Colourbox.