Vand: glassets ven eller fjende?
Glas er skrøbeligt og går let i stykker, når vi taber det. Derfor arbejder forskere på at udvikle nye metoder til at forbedre styrken af glas. Og muligvis kan man med noget så simpelt som vanddamp opnå samme effekt som med traditionelle metoder til hærdning af glas.
Af Elsebeth J. Pedersen og Morten M. Smedskjær
Glas er et helt uundværligt materiale i moderne teknologi og arkitektur. I bygninger bruges glas til alt fra energibesparende ruder til isoleringsfibre. I elektronik er glas en nøglekomponent i skærme til smartphones, tablets og fjernsyn. I medicinsk udstyr og laboratorier spiller glas en central rolle, fordi det er kemisk stabilt og let at rengøre. I den grønne omstilling bruges glas i både solceller og vindmøller.
Men jo mere vi integrerer glas i vores hverdag – og jo mere vi forventer, at det skal kunne holde til – desto vigtigere bliver dets styrke. Et tagvindue i et hus må ikke splintres ved haglvejr. En mobilskærm skal kunne overleve et fald på fortovet. Og ville det ikke være rart, hvis bilruder blev stærke nok til at modstå et stenslag?
Derfor er forskningen i stærkere glas ikke bare et spørgsmål om komfort, men i særdeleshed også et spørgsmål om sikkerhed, funktionalitet og fremtidens teknologiske muligheder. Stærkere glas kan også gøres tyndere, hvilket vil mindske dets store CO2-aftryk.
Den praktiske styrke af glas
Når vi beskriver styrken af glas, skelner vi oftest mellem den teoretiske styrke og den praktiske styrke. “Rygraden” i glas består af et netværk af atomer, der er bundet sammen af kovalente bindinger (se boks). Disse bindinger er enormt stærke, hvilket betyder at der skal meget energi til at skille atomerne fra hinanden. Den teoretiske styrke af glas er baseret på netop den energi, der skal til for at skille atomerne ad, og derfor er den meget høj for glas. Omvendt er den praktiske styrke forholdsvis lav. Det betyder, at der reelt ikke skal så stor en ydre kraft til at bryde disse bindinger og dermed få glasset til at revne og gå i stykker.
Årsagen til dette finder vi i glassets overflade. Her befinder sig et væld af mikroskopiske revner, som bliver skabt under produktion og håndtering, men som ofte er så små, at de ikke kan ses med det blotte øje. Når glasset får et hårdt slag, er det netop disse revner, som kraften fra slaget koncentreres omkring, hvilket gør at bindingerne bliver brudt, og revnen vokser.
Når revnen når over en kritisk længde, vil den fortsætte med at vokse spontant, altså uden at vi tilføjer yderligere energi. Det sker, fordi energien, der skal til at danne en ny overflade, bliver mindre end den energi, vi frigiver ved at bryde glassets bindinger. Et eksempel, de fleste kender, er fra et stenslag på en bilrude, hvor det, der starter som et lille slag, over tid løber på tværs af hele ruden.
Denne proces vil for de fleste glastyper blive forstærket af vand, da det “angriber” spidsen af glassets revne og sænker energien, der skal til at bryde de omkringliggende bindinger. Det kaldes stress-korrosion og betyder, at tilstedeværelsen af vand, oftest i form af fugtighed i luften, sænker den kraft eller energi, der skal til for at få revnen til at vokse, og dermed sænker den praktiske styrke af glasset.
Derfor forskes der intenst i at øge den praktiske styrke af glas, blandt andet i vores forskningsgruppe på Aalborg Universitet.
Glastilstanden
Glasmaterialer dannes ved hurtig afkøling af en væske. Glas er altså ikke bare et materiale med én kemisk sammensætning, men kan bedre forstås som en tilstandsform. Alle materialer, der kan smeltes, kan således omdannes til glastilstanden, hvis de nedkøles hurtigt nok til at undgå krystallisering. Glas er derfor et fast stof, hvor atomerne er “frosset fast” i de samme positioner som i den forudgående væsketilstand. Hvor krystaller og metaller har en meget ordnet struktur med atomerne placeret på rad og række, er strukturen af glas derimod uordnet (amorf).
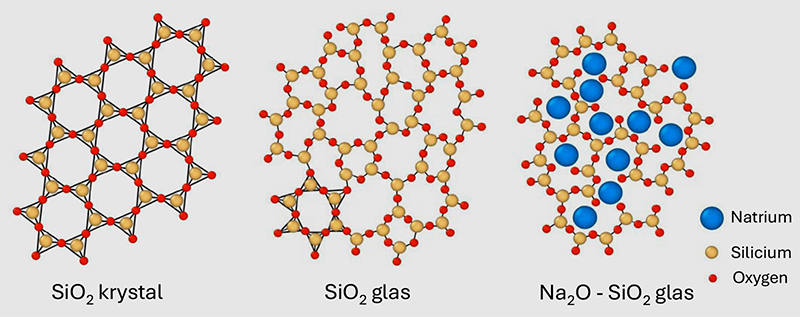
Figuren ovenfor viser denne forskel på krystal- og glasform samt en modificeret glasform for forbindelsen siliciumdioxid (SiO2). En ordnet struktur er nemmere at beskrive, da vi for en perfekt krystal blot skal kende den såkaldte enhedscelle, altså kun en lille del af strukturen, før vi kan beskrive det hele. En uordnet struktur er derimod sværere at beskrive, da vi ikke har de samme gentagelser i strukturen – om end lokale områder i glasset godt kan have en krystallignende struktur, som det fremgår af figuren.
Det meste glas, vi møder i dagligdagen, er såkaldt silikatglas, der typisk fremstilles af kvartssand (siliciumdioxid, SiO2), soda (natriumkarbonat, Na2CO3) og kalk (calciumkarbonat, CaCO3), samt mindre mængder magnesiumkarbonat (MgCO3) og aluminiumoxid (Al2O3).
Når massen smeltes for at fremstille glas, omdannes karbonaterne til oxider under frigivelse af CO2 (for eksempel Na2CO3 → Na2O + CO2), hvilket medvirker til den store CO2-udledning ved glasproduktion. I silikatglas udgør SiO2 den såkaldte netværksdanner, der med sine kovalente oxygenbroer (Si-O-Si bindinger) danner et tredimensionelt netværk. Netværksdanneren er glassets “rygrad”, fordi det nemt kan danne en glasstruktur alene, og derfor er det vigtigste element i glasset.
Na2O, CaO og MgO er modifikatorer i glasset, som bryder de kovalente oxygenbroer og danner ionbindinger i glasstrukturen (for eksempel Si-O … Na, som vist på figuren), hvilket sænker smeltetemperaturen. Langt de fleste elementer i det periodiske system kan indgå som modifikator i glas. Al2O3 er et såkaldt mellemstof, hvilket betyder at det kan indgå i glasset som både netværksdanner og modifikator, alt efter hvad resten af glasset består af. Det kan kun meget vanskeligt danne glas i sig selv, men kan indgå i glassets kovalente netværk, hvis der er modifikatorer til stede.
Traditionelt gøres glas stærkere ved at efterbehandle det ved en såkaldt hærdningsproces. Denne hærdning skaber en spændingsprofil i glasset, hvilket medfører at der skal mere kraft til at danne de mikroskopiske revner. Men hærdningen koster for både pengepung og miljø, da metoderne kræver høje temperaturer. De er dog nødvendige, da alternativet er værre; lavere praktisk styrke af glasset, og dermed glas der lettere går i stykker og skal udskiftes.
Selvhelende glas åbner for spændende spørgsmål
I 2019 opdagede vi på Aalborg Universitet sammen med vores samarbejdspartnere en ny glastype, der har rekordhøj praktisk styrke, fordi det er meget modstandsdygtigt overfor at danne revner, og som ovenikøbet har evnen til at hele sig selv, hvis man blot behandler glasset med vanddamp. Glasset har dog to væsentlige ulemper, nemlig at den kemiske holdbarhed er ekstremt lav, og at glasset indeholder et dyrt råstof (cæsiumoxid). Glasset kan derfor i sig selv ikke bruges til kommercielle formål.
Opdagelsen åbnede dog op for en række spændende spørgsmål. For hvad er årsagen til, at lige præcis denne type glas reagerer sådan med vanddamp? Og hvad vil der ske, hvis vi udsætter andre glastyper for den samme behandling? Med disse spørgsmål begyndte vores rejse på at udvikle et glas, der havde samme positive effekt ved reaktion med vand, men med markant højere kemisk holdbarhed. Det har vi gjort gennem et forskningsprojekt finansieret af Danmarks Frie Forskningsfond.
Når vi fremstiller “et nyt glas”, betyder det, at vi har smeltet et glas med en specifik kemisk sammensætning. For selvom vinduesglas har bestået af de samme tre primære råstoffer i flere århundreder, så kan langt de fleste elementer i det periodiske system faktisk indgå i en glaskomposition. Det er derfor ikke så ligetil at designe nye glas, da mulighederne er enorme.
Det teoretiske antal mulige glaskompositioner, vi kan lave, er vurderet til 10 oktilliarder (1052). Det gigantiske tal fremkommer, fordi vi kan tilføje så mange forskellige elementer fra det periodiske system, og fordi vi kan blande dem i et væld af sammensætninger. Af denne grund er udviklingen af nye glastyper i høj grad en “trial and error” proces, hvor man i en gentagen proces justerer lidt på sammensætningen, tester egenskaberne, justerer osv.
Termisk og kemisk hærdning
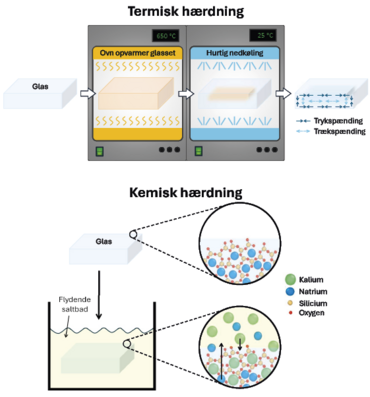
Glas kan opnå en højere styrke ved termisk eller kemisk hærdning.
Ved termisk hærdning opvarmes glasset (til omkring 650 °C for vinduesglas), hvorefter overfladerne nedkøles hurtigt. Dermed trækker overfladerne sig sammen hurtigere end glassets kerne, hvilket skaber en trykspænding i glassets overflade, som gør det vanskeligere at danne mikroskopiske revner.
Ved kemisk hærdning sænkes glasset ned i et flydende saltbad (for eksempel kaliumnitrat, KNO3) ved en temperatur på omkring 400 °C. Den højere temperatur øger bevægeligheden af atomerne nok til, at natrium-atomer i glassets struktur kan byttes ud med de større kaliumatomer i saltbadet, men uden at de stærkere bundne siliciumatomer bevæger sig. På grund af størrelsesforskellen af natrium- og kalium-atomer skabes der også ved denne behandling en trykspænding i glassets overflade.
Kemisk hærdning skaber en kraftigere, men mindre dyb trykspænding i overfladen af glasset, og benyttes derfor typisk til tyndere glasstykker som telefonskærme, hvorimod større glasstykker såsom vinduer eller bilruder typisk hærdes termisk.
Nye lovende glaskompositioner
Vores forskning har vist, at komponenter som boroxid (B2O3), aluminiumoxid (Al2O3) og fosforoxid (P2O5), der alle kan indgå i de kovalente bindinger, der udgør glassets rygrad, er essentielle at have (én eller flere af) i glasset for at opnå en positiv effekt af vandbehandlingen. Hvis man kombinerer det med en større alkali-ion, for eksempel kalium, øger det igen sandsynligheden for en positiv effekt. Men det er ikke uden udfordringer at ændre glassets sammensætning. Der er risiko for, at der dannes krystaller, og/eller at den smeltede masse deler sig i flere faser – i lighed med, når man blander vand og olie. Det fører til en række nye problemer, når den smeltede masse køles og bliver til glas.
På trods af disse udfordringer er det lykkedes os at udvikle flere glaskompositioner, der kombinerer relativ høj kemisk holdbarhed med positiv effekt af vandbehandlingen. Den positive effekt ses ved, at glasset bliver mere modstandsdygtigt overfor revner, og at de skader, der faktisk findes i glasset, bliver mindre efter kontakt med vanddamp, altså en form for selvheling.
Vores forskning viser altså, at når vand bruges rigtigt, og på den rigtige glaskomposition, kan det bruges til at styrke glas.
Selve vandbehandlingen er meget simpel. Ønsker vi en mild behandling af glasset, foregår det i et klimaskab hvor temperatur (typisk 25-80 °C) og relativ fugtighed (typisk 40-80%) kan indstilles præcist. Det er derfor vanddampen i luften af kammeret, der reagerer med glasset. Ønsker vi en mere ekstrem behandling, bruger vi en autoklave, hvor vanddampen også skaber et tryk omkring prøven. Her behandler vi typisk ved 105-140 °C ved 100% relativ fugtighed. Den mildere behandling i klimaskabet kræver typisk en længere behandlingstid på mindst 24 timer, mens behandling i autoklave typisk er på maksimalt 24 timer, og helt ned til ½ time.
Fra laboratoriet til produktion
Udover forskningen på universiteter arbejder den amerikanske glasproducent Corning Inc. også på metoden. Corning Inc. er verdens førende producent af specialglas til blandt andet mobiltelefoner og optiske fibre. De har vist, at deres udviklede glaskompositioner danner trykspændinger i overfladen efter behandling med vanddamp. Denne spændingsprofil minder om den, der dannes ved kemisk hærdning (se boksen: Termisk og kemisk hærdning), blot med en lidt lavere styrke.
Hvordan vandet danner denne spændingsprofil ved vi stadig ikke med sikkerhed, men vi ved, at det medvirker til den øgede brudstyrke af disse glas. Corning Inc. har patenteret dele af denne forskning, og ved en international glaskonference i foråret 2025 løftede de sløret for, at de arbejder intensivt på at kunne frigive et glasprodukt, der er efterbehandlet med vanddamp.
Dette er banebrydende på flere områder, mest af alt fordi vandbehandlingen er langt mere klimavenlig end den kemiske hærdning, da temperaturen er lavere, og vand er det eneste råmateriale. Men ifølge vores forskning også fordi glasset kan reagere med fugt fra luften efter behandlingen. Når behandlingen laves, øges temperaturen, og eventuelt også trykket, for at fremskynde processen, men reaktionen kan også ske ved langt lavere temperaturer, blot langsommere.
For nogle glastyper betyder det, at glasset gradvist vil blive stærkere blot ved at ligge på for eksempel skrivebordet ved siden af os. Og ikke nok med det: Revner og ridser i overfladen vil være mere modtagelige overfor denne reaktion – både de mikroskopiske revner, der opstod under produktionen, og de ridser, der siden er kommet til ved brug, for eksempel af vores mobiltelefon. Det kan betyde, at de svageste punkter i glasset kan forstærkes blot ved at reagere med fugtigheden i luften omkring os.
Hvis vi blot designer den rigtige glaskomposition, kan vand altså sagtens være glassets ven – selv, når det sidder på en mobiltelefon. ♦
Eksperimentelle metoder
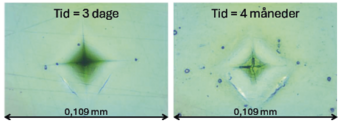
Hvordan undersøger man, hvor meget kraft der skal til, før der dannes overfladerevner i glas? Eller hvordan glassets struktur ændrer sig, når vi behandler glasset med vand? Det kræver selvsagt forskellige eksperimentelle metoder. Meget af dette udstyr har vi selv til rådighed i laboratoriet, for eksempel en indenter, også kendt som en hårdhedsmåler. En indenter laver små (mikroskopiske) aftryk i glasset med en diamantspids. Ved efterfølgende at undersøge størrelsen og formen af disse aftryk, kan vi bestemme, hvor hårdt glasset er, samt hvor stor kraft der skal til, før glasset revner. Vi kan også se på mærkerne før og efter en behandling, for at undersøge om behandlingen har gjort dem mindre.
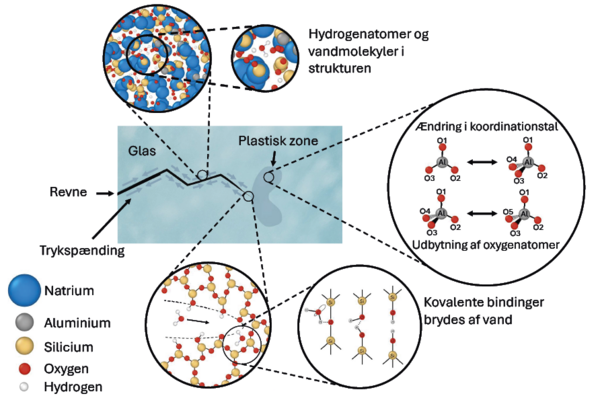
Der kan ofte også være behov for større og dyrere udstyr, end vi selv har til rådighed i laboratoriet. Det kan være en røntgen- eller neutronlinje til at karakterisere glassets struktur, dvs. hvordan atomerne sidder i strukturen. Med dette udstyr kan vi for eksempel måle, hvor mange oxygenatomer der sidder rundt om netværksdanneren (koordinationstal), eller hvor stor afstand der er mellem forskellige atomer i glasset (bindingslængde).
Ved behandling med vanddamp undersøger vi for eksempel, hvor mange og hvilke atomer der ændrer koordinationstal som følge af behandlingen, da mange ændringer betyder en mere “fleksibel” struktur. Ændringer i bindingslængder kan give os information om, hvordan vandet binder til glasnetværket – altså hvor godt det “sidder fast”, eller hvor let det er at fjerne igen. Det er meget informativt, da vandet gerne skal blive i strukturen for at bibeholde den positive effekt af behandlingen, og ikke dampe af ved små stigninger i temperaturen, for eksempel hvis solen skinner på glasset.