Sådan virker fugles nethinder uden ilt
Nervevæv dør normalt hurtigt, hvis det ikke får ilt. Alligevel fungerer fugles nethinder – som hører til blandt de mest energikrævende væv i dyreriget – permanent uden ilt. Otte års forskning har nu løst det mysterium.
Af Peter F. Gammelby
I et studie publiceret for nyligt i Nature, viser et internationalt forskerhold ledet fra Aarhus Universitet, hvordan fugle har løst et biologisk paradoks: Hvordan kan fugles nethinder fungere uden blodkar og dermed uden ilt? Forskerne dokumenterer, at de inderste dele af fugles nethinder får energi ved at omdanne glucose med en hidtil uset effektivitet. Samtidig vælter studiet en mangeårig antagelse om funktionen af en mystisk struktur i øjet, som har undret forskere siden 1600-tallet.
Nethinden kræver masser af energi
Hos de fleste dyr forsynes nervevæv med ilt gennem tætte netværk af små blodkar (kapillærer). Det betragtes som helt afgørende, da nerveceller har et usædvanligt højt energiforbrug. Nethinden, som er en højt specialiseret forlængelse af hjernen, er ingen undtagelse – og forbruger faktisk mere energi end noget andet væv i kroppen.
Fugle udgør imidlertid et paradoks. Deres nethinder mangler blodkar i selve nethindevævet. Denne egenskab menes at forbedre synsskarpheden, fordi blodkar spreder lyset på vej til sansecellerne. Men hvordan nethinden overlever uden blodforsyning har hidtil været ukendt.
»Vores udgangspunkt var simpelt,« siger Christian Damsgaard, førsteforfatter på studiet og lektor ved Institut for Biologi, Aarhus Universitet. »Ud fra alt, hvad vi ved om fysiologi, burde dette væv ikke kunne fungere.«
Vejen til en løsning på mysteriet viste sig at være alt andet end simpel. Det har taget Damsgaard og et stadigt voksende forskerhold – primært fra Aarhus Universitet – otte år at nå frem til de resultater, som nu er offentliggjort.
Ingen ilt dér, hvor man troede
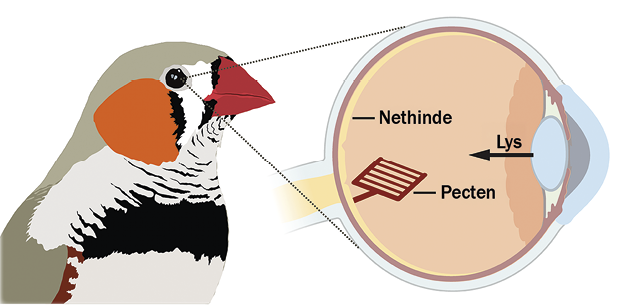
I århundreder har den dominerende forklaring været, at en struktur kaldet pecten oculi – et kamformet organ med masser af blodkar, der rager ind i øjets glaslegeme – leverer ilt til nethinden. Strukturen har været kendt siden 1600-tallet, men forklaringer på, hvad den præcist laver derinde i øjet, har hidtil været baseret på antagelser. Det skyldes ikke mindst, påpeger forskerne, at ingen tidligere har kunnet måle iltniveauerne direkte i fugles nethinder under normale fysiologiske forhold.
»Det er teknisk ekstremt udfordrende,« siger studiets seniorforfatter Jens Randel Nyengaard, der er læge og professor ved Institut for Klinisk Medicin, Aarhus Universitet.
»Man skal holde dyret i stabile, fysiologisk normale tilstande, samtidig med at man udfører meget følsomme målinger.«
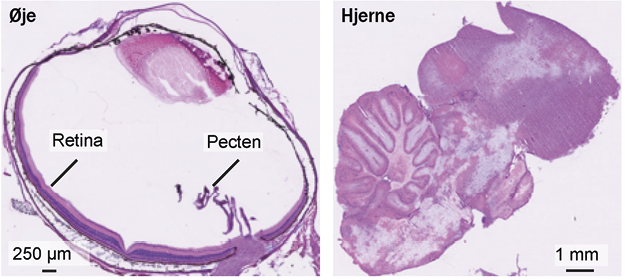
I 2020 lykkedes det forskerholdet at gøre netop dette, takket være et samarbejde med dyrlæge og ekspert i anæstesi, lektor Catherine Williams Institut for Husdyr- og Veterinærvidenskab på Aarhus Universitet. Og resultaterne var uventede: Pecten oculi leverer slet ikke ilt til nethinden. Målingerne viste, at de inderste lag af nethinden næsten ikke modtager ilt, og at omtrent halvdelen af nethindevævet slet ikke modtager ilt.
Hvert svar gav nye spørgsmål
Hvis nethinden ikke får ilt, hvordan producerer den så tilstrækkelig energi til at fungere?
For at besvare det spørgsmål iværksatte forskerne et flerårigt studie, der kombinerede fysiologi, molekylærbiologi, billeddannelse og dataanalyse. Fremdriften var langsom, dels fordi datamængderne var uhyre komplekse og dels på grund af COVID-19-pandemien, som begrænsede forskernes adgang til laboratorierne. Ved hjælp af en metode kaldet spatial transcriptomics kortlagde forskerne aktiviteten af tusindvis af gener i tynde snit af nethinden, hvilket gjorde det muligt at se, hvilke metaboliske processer der var aktive hvor.
»Vi kiggede ikke på ét eller to gener, men på 5.000 til 10.000 gener på én gang, hver knyttet til en præcis position,« siger Christian Damsgaard. »Det gav os en slags molekylært GPS-system.«
Dataene afslørede et markant mønster: Gener involveret i forbrænding af glucose uden ilt (anaerob glykolyse) var stærkt aktive i de iltfri inderste lag af nethinden. Anaerob glykolyse giver dog omkring 15 gange mindre energi per glucosemolekyle, end iltbaseret stofskifte gør.
»Det rejste endnu et spørgsmål,« siger Jens Randel Nyengaard.
»Hvordan kan et af kroppens mest energikrævende væv overleve på så ineffektiv en proces?«
En ny rolle for en gammel struktur
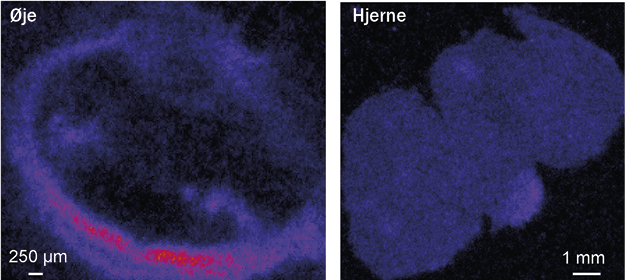
Svaret kom gennem et samarbejde med eksperter i metabolisk billeddannelse – altså scanninger, der visualiserer kroppens stofskifte. Ved hjælp af radioaktiv mærket glucose kunne forskerne vise, at fugles nethinder optager glukose i langt højere grad end resten af hjernen. Det førte forskerne tilbage til pecten oculi, altså det kamformede organ inde i øjets glaslegeme.
Ved at analysere deres spatial transcriptomics-data igen opdagede forskerne, at pecten oculi indeholder en masse transportproteiner for glucose og mælkesyre. Strukturen fungerer altså som en port for stofskiftet: Den leverer store mængder glucose ind i nethinden og fjerner mælkesyre – som er et affaldsprodukt fra anaerobt stofskifte – tilbage til blodbanen.
»Pecten er ikke en iltforsyning. Det er et transportsystem for brændstof ind og affald ud,« forklarer Jens Randel Nyengaard.
Opdagelsen ændrer grundlæggende forståelsen af en struktur, som har været misfortolket i århundreder.
»Vi vælter i praksis ét korthus og erstatter det med et andet. Jeg kalder det et korthus, fordi videnskabelige resultater ikke er hugget i sten. Nye fund kan føje ny viden til. Sådan udvikler videnskaben sig,« tilføjer Jens Randel Nyengaard.
Evolutionære og medicinske perspektiver
Forskerne peger på, at fraværet af ilt og blodkar i nethinden sandsynligvis giver en optisk fordel og bidrager til skarpere syn. Genetiske analyser af fuglenes evolution tyder på, at denne egenskab opstod i dinosaurernes slægtslinje, som senere gav ophav til nutidens fugle. Studiet er ren grundforskning, men forskerne fremhæver, at resultaterne kan have bredere perspektiver.
»Når mennesker får blodpropper, bliver vores væv skadet, fordi det får for lidt ilt, og der ophobes affaldsstoffer. I fuglens nethinde ser vi et system, der håndterer iltmangel på en helt anden måde,« siger Jens Randel Nyengaard.
Og tilføjer: »Hos fugle har naturen løst et fysiologisk problem, som gør mennesker syge. Vi håber, at den nye indsigt kan inspirere nye måder at tænke over, hvorfor væv svigter ved iltmangel, og hvordan sådanne sygdomme kan behandles en gang i fremtiden.« ♦