På vej mod faststofbatterier
I fremtidens grønne energisystem bliver der brug for nye typer af batterier, der kan imødegå begrænsningerne i det traditionelle litium-ion-batteri. Et lovende bud er faststofbatterier, og opdagelsen af nye mekanismer, der skaber god ledningsevne i uorganiske stoffer, kan hjælpe udviklingen på vej.
Af Mads B. Amdisen, Therese S. S. Kjær, Lasse G. Kristensen, Jakob B. Grinderslev, Lasse N. Skov og Torben R. Jensen
I den grønne omstilling spiller batterier en væsentlig rolle, fordi de tilbyder en mulighed for at lagre og udnytte den elektriske strøm, der bliver produceret af solceller og vindmøller, til mange forskellige formål – ikke mindst i elbiler. Mange mener, at det litium-ion-batteri, vi kender i dag, er tæt på fuldt optimeret, og at energiindhold, effekt osv. næppe kan forbedres væsentligt. Derfor forskes der intenst i at udvikle helt nye typer af batterier. En lovende type er faststofbatterier, der er opbygget udelukkende af faste, uorganiske materialer og gerne baseret på divalente metaller som magnesium og calcium.
Fordele ved faststofbatterier
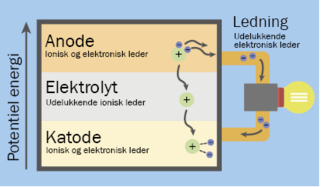
Et faststofbatteri består i lighed med et traditionelt litium-ion-batteri af to elektroder (kaldet anode og katode) samt en elektrolyt. Elektroderne kan forbindes med en ledning, så man kan udnytte den strøm, der dannes. Et faststofbatteri adskiller sig fra litium-ion-batterier ved, at elektrolytten er et fast stof. Elektrolytten tillader kun kationer såsom litium (Li+), natrium (Na+) eller magnesium (Mg2+) at trænge igennem, mens elektroner ikke kan passere. Elektrolytten er altså en elektrisk isolator.
I et litium-ion-batteri består elektrolytten af organisk væske eller polymer samt et litiumsalt, typisk LiPF6. De organiske opløsningsmidler udgør en risiko, da de er brandfarlige. I et faststofbatteri fungerer elektrolytten desuden som en fysisk separator mellem elektroderne, så batteriet ikke kortslutter, mens man i et litium-ion-batteri skal indsætte en semipermeabel plastikmembran for at undgå dette. En elektrolyt af uorganisk faststof kan ofte fungere stabilt i et større temperaturområde end en organisk væske.
Årsagen til den forskningsmæssige interesse i faststofbatterier er, at man forventer, at de i forhold til traditionelle litium-ion-batterier kan være mere sikre (dvs. mindre brandfarlige), have en længere levetid samt højere energitæthed, da en faststofelektrolyt kan tillade brugen af en metalanode. En elektrolyt af organisk væske er ikke kompatibel med en litium-metalanode, fordi der kan dannes nåleformede litiumkrystaller, som kan kortslutte batteriet. Derfor bruges grafit som anode i litium-ion-batterier. Det giver batteriet stor stabilitet, men lille energiindhold.
Metaller og energiindhold
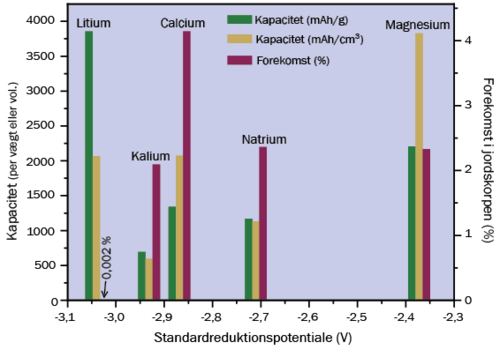
Figuren viser energikapaciteten per vægt (grøn søjle) og per rumfang (gul søjle) af forskellige metaller samt, hvor stor andel disse udgør i vægtprocent af jordskorpen (rød søjle). Litium forekommer i økonomisk interessante mængder få steder på jorden, hvorimod natrium (Na), magnesium (Mg) og calcium (Ca) findes nærmest overalt. Metallerne er ordnet på 1.-aksen efter deres standardreduktionspotentialer. Jo mere negativt, det er, jo større kan energiindholdet i batteriet blive. Bemærk også, at Mg og Ca bærer to elektroner og Li og Na kun én.
Nye opdagelser baner vejen for nye elektrolytter
I processen med at udvikle nye typer af batterier er det væsentligt, at disse bliver baseret på råstoffer, der er let tilgængelige, samt at tænke i genanvendelse. En fordel ved det velkendte blybatteri er, at det er let at skille ad og genbruge komponenterne. Det forholder sig lige modsat med Li-ion-batteriet, der er meget vanskeligt at genbruge. Hvis nye typer batterier skal være mere bæredygtige er det derfor meget vigtigt at de har lukkede materialekredsløb, hvor alt kan genbruges.
I forhold til tilgængeligheden af råstoffer, så findes der langt mindre tilgængeligt litium i jordskorpen end for eksempel natrium, magnesium eller calcium, som også geografisk er meget mere velfordelt (se boks). Litium udvindes primært i Kina, Chile og Australien, og det er en udfordring i forhold til de politisk-strategiske ambitioner om “lokal” batteriproduktion i Norden og i Europa.
En af de største udfordringer ved at udvikle helt nye faststofbatterier har længe været at designe og fremstille nye kemiske stoffer til elektrolytter med høj ionledningsevne ved stuetemperatur, som samtidig er en isolator for elektrisk strøm. Denne opgave er overkommelig for monovalente kationer som Li+ og Na+, men ekstremt vanskeligt for divalente kationer som Mg2+ og Ca2+, fordi de binder sig stærkere til omgivelserne.
I vores forskningsgruppe ved Institut for Kemi og iNANO, Aarhus Universitet har vi knækket koden ved at opdage nye strukturelle og fysiske fænomener, der skaber høj ionledningsevne. Det har vi udnyttet til at designe adskillige nye kemiske forbindelser, der leder kationer med en ny mekanisme, der ikke tidligere er beskrevet, og som virker både på det atomare niveau og på nanometer-skala. Med disse nye stoffer har vi sat nye standarder og flere verdensrekorder for di- og trivalente kationer og skabt basis for en metodik til rationelt design af elektrolytter til brug i faststofbatterier.
Struktur af nye stoffer med høj ionledningsevne
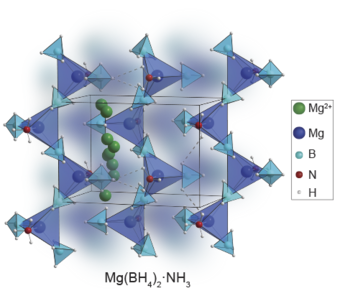
Figuren viser strukturen af den nye uorganiske forbindelse Mg(BH4)2 · NH3 (den indtegnede kasse viser “enhedscellen” dvs. den grundstruktur, der gentages i det krystallinske materiale). Denne forbindelse leder kationer med en ny mekanisme, der ikke tidligere er beskrevet, hvor neutrale molekyler (her NH3) hjælper med at føre Mg2+ igennem det faste stof. Forbindelsen har en lagdelt struktur, idet de enkelte kæder i strukturen holdes sammen af svage dihydrogenbindinger, der opstår fordi delvist positivt ladede hydrogenatomer på ammoniakmolekyler (NH3) binder sig til delvist negativt ladede hydrogenatomer på borhydrid-komplekser (BH4-).
Der er vist nogle eksempler på sådanne dihydrogenbindinger som stiplede linjer på figuren. De svage dihydrogenbindinger gør strukturen meget fleksibel, hvilket gør det muligt for kationer (Mg2+) at trænge igennem, og de er vist som grønne kugler på figuren. Dihydrogenbindingerne har i øvrigt samme bindingslængde (cirka 0,2 nm) og bindingsstyrke (cirka 20 kJ/mol) som de svage hydrogenbindinger, der findes i alt biologisk materiale som proteiner og membraner, og som er med til at give en fleksibel struktur.
Ved Institut for Kemi og iNANO, Aarhus Universitet har vi lavet en række andre lignende nye kemiske forbindelser med meget høj kationledningsevne. De har det tilfælles, at man kan lave blandinger af dem, som har lave smeltepunkter. Disse blandinger kan stabiliseres med ikke-reaktive og elektrisk isolerende nanopartikler såsom MgO eller Al2O3.
Fleksibel struktur giver høj ledningsevne
Vores opdagelse tager udgangspunkt i et nyt uorganisk stof, vi har lavet, som har den kemiske sammensætning Mg(BH4)2· NH3. Det er et fast, krystallinsk stof med en lagdelt, fleksibel struktur. Den fleksible struktur skyldes, at strukturen er holdt sammen af svage di-hydrogen-bindinger imellem ammoniak-molekyler (NH3) med delvist positivt ladede hydrogenatomer og borhydrid-komplekser (BH4-) med delvist negativt ladede hydrogenatomer.
Dette uorganiske, krystallinske stof har vist sig at have en meget høj ledningsevne for magnesiumioner. Det skyldes en hidtil ukendt mekanisme, hvor neutrale molekyler (her NH3) hjælper Mg2+ igennem det faste stof. Det skyldes også, at strukturen er fleksibel, fordi den er holdt sammen af svage dihydrogenbindinger. Der er således tale om en generel mekanisme, der virker i en lang række stoffer med en tilsvarende struktur.
Den næste interessante opdagelse er, at vi kan øge kationledningsevnen betydeligt (ofte mere end 100 gange), når vi laver blandinger (kompositter) af to næsten ens udgaver af denne type uorganiske, krystallinske forbindelser. Det gælder for eksempel Mg(BH4)2· NH3 og Mg(BH4)2 · 2NH3, hvor forskellen altså er et ekstra ammoniakmolekyle på den ene forbindelse.
Ulempen ved sådanne blandinger i forhold til at anvende dem i batterier er, at kompositter ofte har et lavere smeltepunkt end de rene stoffer. Det er også tilfældet her, idet en 1:1-blanding af de to nævnte stoffer smelter ved 55 °C, mens de rene stoffer smelter ved cirka 100 °C, hvilket ikke er ideelt i forhold til anvendelse i batterier. Men den udfordring har vi også fundet en løsning på: Nemlig at tilsætte nano-partikler (af for eksempel magnesiumoxid) med stort overfladeareal til blandingen. Dette giver mekanisk stabilisering af materialet.
Nye kemiske forbindelser
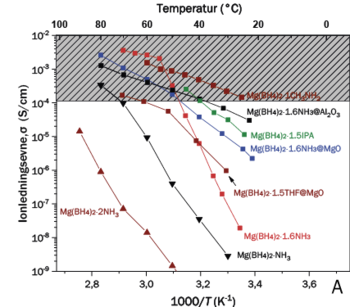
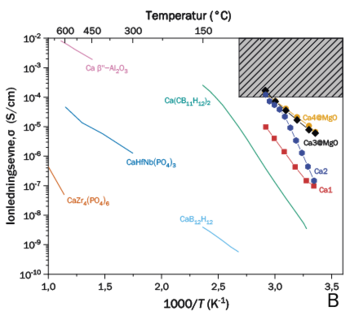
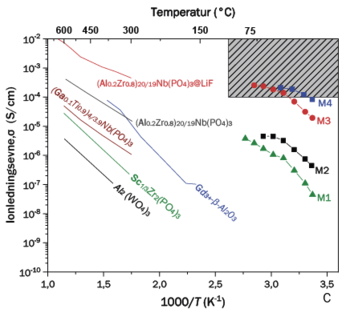
De tre figurer viser kationlednings-evnen for nye (A) magnesium (Mg2+), (B) calcium (Ca2+) og (C) trivalente (M3+) kationledere som funktion af temperaturen. De grå skraverede områder angiver ledningsevne og temperatur-område, hvor det er realistisk at lave et faststofbatteri, der kan anvendes ved moderat temperatur.
Bemærk, at ledningsevne, σ, som regel angives med en logaritmisk 2.-akse og som funktion af reciprok temperatur (1/T). Hvis det bliver en ret linje, så følger ledningsevnen Arrhenius lov, ln(σ) = lnA – EA / RT, og det betyder ofte, at der kun er én mekanisme for kationledningen i dette temperaturområde. Hældningen af linjen angiver aktiveringenergien, EA, for processen. Man kan ikke tage logaritmen til en fysisk enhed, så ln(σ) er enhedsløs, og hældningen af linjen, EA, får enheden J/mol, da gaskonstanten R har enheden J/(mol · K). Jo mindre aktiveringsenergien er, jo mere vandret er linjen, og det giver højere kationledningsevne ved lavere temperaturer. Det kan gøre det muligt at lave en nye type batteri, der både virker ved stuetemperatur og i frostvejr på en vinterdag. På 2.-aksen står S for den afledte SI-enhed siemens, som er det samme som S = ohm−1 = Ω−1.
Data angivet som punkter er målt på Institut for Kemi og iNANO i tre igangværende forskningsprojekter, og data angivet som streger er fundet i den kemiske litteratur. Særligt ledningsevnen for calcium og trivalente ioner (M3+) adskiller sig ved at være ekstremt høj ved meget lavere temperaturer sammenlignet med alle andre kendte forbindelser. Figur (A) og (B) indeholder også data for nye nano-kompositter, som indeholder nanopartikler af magnesiumoxid (MgO) eller aluminiumoxid (Al2O3). Læg mærke til, at de nye kemiske forbindelser udviklet i Aarhus har langt højere kationledningsevne i et relevant temperaturområde end andre kendte stoffer, og de er også elektrisk isolerende.
Rationelt design af nye elektrolytter
Med disse tre trin: 1) design af en uorganisk, krystallinsk forbindelse med god ledningsevne, 2) dannelse af kompositter ud fra disse og 3) stabilisering af kompositterne ved hjælp af nanopartikler har vi nu en systematisk metodik til at udvikle nye interessante materialer til brug i faststofbatterier.
Fordelene ved vores nye nano-komposit-materialer er, at de har ekstremt høj kationledningsevne ved moderat temperatur, meget høj mekanisk stabilitet og forbedret termisk stabilitet i forhold til de rene stoffer.
Det er også lykkedes os at lave et nyt magnesiumbatteri med en af de nye nano-kompositter. I dette batteri består elektrolytten af en komposit, der er en blanding af de to kemiske forbindelser Mg(BH4)2 og NH3 i forholdet 1:1,6 og stabiliseret med nanopartikler af magnesiumoxid (MgO).
Batteriets anode består af metallisk magnesium, mens katoden består af Mg0,2TiS2, hvor mængden af Mg2+ ændres ved opladning og afladning. Batteriets spænding er på 1,2 V, og det kan oplades og aflades 60 gange. Vi forventer, at vi med yderligere optimering – for eksempel af grænsefladen mellem elektrolytten og anode/katode – kan forbedre batteriets energiindhold og levetid betydeligt.
Faststof-magnesium-batterier lavet af uorganiske stoffer findes der meget få af i verden, og vores forskning viser således, at det ud fra grundlæggende kemisk forståelse er muligt at designe helt nye funktionelle materialer, som kan danne grundlag for helt nye faststofbatterier.
Opbevaring af vedvarende energi og energitab
En af de mest grundlæggende naturlove, termodynamikkens anden hovedsætning, indebærer, at hver gang vi omdanner energi fra en form til en anden, så mister vi noget energi i form af varme. Det forklarer, at vi ikke kan lave en evighedsmaskine, fordi der aldrig er noget, der er 100 % effektivt. Alene ved genopladning af et litium-ion-bilbatteri mister man således 5-20 % af den tilførte strøm, som omdannes til varme.
Når man kører mistes også energi i form af varme ved frigivelse af strøm fra batteriet og omdannelse til mekanisk energi via en elmotor. Hvis vi i stedet ser på energiforbrug per kørt kilometer, og antager, at en elbils og en benzinbils energiforbrug er hhv. 160 Wh/km og 20 km/l benzin, så er elbilen ca. 2,5 gange mere energieffektiv end benzinbilen.
En bil kan også køre på dihydrogen (H2), som man kan producere ved elektrolyse, hvor man spalter vand til hydrogen og oxygen med en effektivitet på 75 til 90 %. Hydrogen kan så efterfølgende omdannes til strøm i en brændselscelle med en effektivitet på 30 til 50 %. Den resterende energi bliver til varme, som kan bruges til opvarmning af bilen om vinteren.
Spaltning af vand til hydrogen og oxygen er udgangspunktet for såkaldt Power-to-X, idet den fremstillede dihydrogen kan anvendes til produktion af ammoniak (NH3), methanol (CH3OH) eller metan (CH4). De ekstra procestrin medfører yderligere energitab, hvorfor det er mindre energieffektivt at producere disse end ren hydrogen. Ydermere har udnyttelsen af disse kemikalier også lav effektivitet, hvis de forbrændes i en forbrændingsmotor eller spaltes tilbage til hydrogen, som så kan bruges i en brændselscelle.
Batterier og energieffektivitet
Interessen i nye batterityper er som allerede antydet drevet af behovet for at erstatte vores afhængighed af fossile brændstoffer med noget mere bæredygtigt. Fossilt brændstof har så højt energiindhold, at vi har tilladt os at behandle det på en ineffektiv måde. Vi brænder det bare af og omdanner det herved til varme, som er kendt som den ringeste af alle energiformer.
Sagt på en anden måde forsvinder varme let “ud mellem fingrene” på os, og den er vanskelig at opbevare og omdanne på en effektiv måde til energiformer af højere kvalitet, såsom strøm. Et kraftværk omdanner således kemisk energi i fossilt brændsel til varme og videre til strøm via en dampturbine med en effektivitet på 30-40 %. Et dansk kraftvarmeværk udnytter overskudsvarme fra processen til fjernvarme, så energieffektiviteten måske kommer op på ca. 90 %.
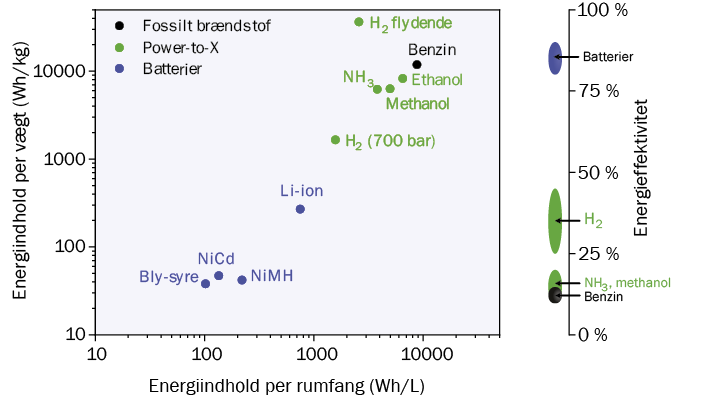
Hvis man sammenligner energiindholdet i kendte batterier med for eksempel benzin, så er det cirka 100 gange mindre. Det er også meget mindre end i kemiske stoffer, man vil lave med “power-to-X”- teknologi, dvs. ammoniak (NH3), methanol (CH3OH) og hydrogen (H2). Fordelen ved power-to-X-kemikalier er, at der kan transporteres og langtidsopbevares langt større energimængder som kemisk energi sammenlignet med strøm i et batteri, som også kan gå tabt over tid ved selvafladning.
Hvis man i stedet ser på energieffektiviteten ved forskellige udnyttelser af “grøn” vedvarende strøm fra vind eller sol, så har batterier en markant højere energieffektivitet end alle andre måder at udnytte strøm på. Hydrogen kan fremstilles med en effektivitet på 75–90 %, men det er kun 30–50 % af den kemiske energi, der kan omdannes tilbage til strøm i en brændselscelle.
Andre power-to-X-kemikalier kan fremstilles fra hydrogen, men der er flere trin i disse processer, og derfor også større energitab. Brænder man dem efterfølgende af i en forbrændingsmotor, er der lille energieffektivitet, dvs. en stor del af den kemiske energi går tabt som varme. Man kan spalte ammoniak tilbage til hydrogen, men det koster også energi.
Batterier i fremtidens energiforsyning
Konklusionen af disse energiovervejelser er nok, at vi aldrig finder én løsning, der kan erstatte benzin, diesel og andet fossilt brændstof, men at vi skal vænne os til en række forskellige løsninger, der hver især har fordele og ulemper. Vi skal også gøre os klart, at vi ikke har uendelige mængder af vedvarende energi fra sol og vind til rådighed, og at disse energistrømme varierer meget, både over året og på døgnbasis.
Derfor er det vigtigt at undersøge både energieffektiviteten og energiindholdet af nye energisystemer og at udvikle nye metoder til energiopbevaring til både kort og lang tid. Nye typer af faststofbatterier kan blive en vigtig komponent i fremtidens langt mere komplekse energisystemer, netop fordi batterier har den allerstørste energieffektivitet. ♦
Energiindhold og energieffektivitet
Fossilt brændstof i form af kul, olie og naturgas er et enormt effektivt energilager, som er nemt at opbevare og transportere og har ekstremt højt energiindhold. Desuden får vi fossilt brændstof foræret fra naturen, og kun en mindre del af det samlede energiindhold forbruges til at grave eller pumpe det op af undergrunden og til raffinering til benzin, diesel, flybrændstof osv. Disse favorable egenskaber ved fossile brændsler gør det til en stor udfordring at erstatte det carbon-baserede energisystem med et “grønt” energisystem baseret på for eksempel sol- og vindenergi.