Forskere jagter forklaring på gådefuldt protein i zebrafisk
Proteinet myoglobin findes hos fisk, fugle og pattedyr. Det er i vores muskler og i vores hjerte, men forskerne aner ikke, hvilken rolle det spiller. Nu har professor Angela Fago med sin gruppe måske endelig fundet en god forklaring.
Af Jeppe Kyhne Knudsen
Efterårssolen står ind ad vinduerne i det hvide laboratorium. Støvpartikler svæver lydløst i det skarpe lys, mens rummet afgiver en svag duft af rengøringsmiddel og sprit.
Sammen med sin ph.d.-studerende Ciska Bakkeren er professor i biologi ved Aarhus Universitet, Angela Fago, ved at samle et specialbygget “løbebånd” til en zebrafisk. En lille lukket vandbane i klar plastik, som ligner et stykke legetøj til en varm sommerdag i haven.
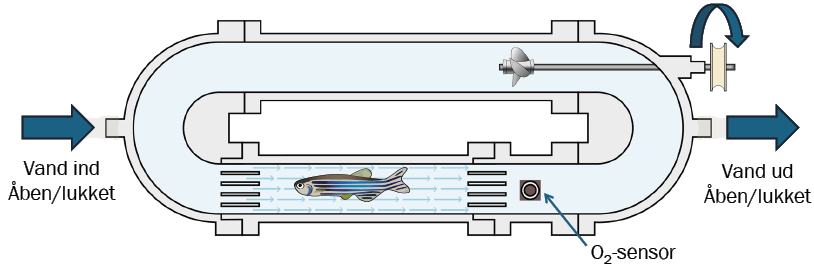
En lille propel er monteret i den ene ende af vandbanen. Den skaber en strøm i vandet, så fisken er nødsaget til at svømme for ikke at blive tvunget tilbage mod et gitter. En lille oxygensensor i vandet måler, hvor meget oxygen fisken optager fra vandet, mens et kamera filmer fisken, så dens hjerteslag kan ses gennem de gennemsigtige skæl.
»Vi bruger “løbebåndet” til at undersøge, hvordan zebrafisks iltforbrug og aktivitet bliver påvirket af, at vi slår et bestemt gen ud hos dem. Et gen, der indeholder opskriften på proteinet myoglobin. Tidligere var der enighed om, at myoglobin, som der er masser af, er afgørende i de fleste dyr for at levere oxygen nok til hjerte og muskler, men vores forsøg tyder på, at det er forkert,« siger Angela Fago.
»Spørgsmålet er, hvilken rolle myoglobin så spiller. Vi ved det ikke med sikkerhed, men vi har en hypotese. Gennem vores forsøg håber vi, at vi kan opklare helt præcist, hvad proteinet laver i muskler og hjerte.«
Mod koldere himmelstrøg
Udenfor laboratoriets store vinduer river et vindstød i universitetsparkens gamle egetræer. Bladene er begyndt at gulne, forberede sig på vinterens komme. Enkelte hvirvler mod jorden. Vintermånederne i Danmark kan sommetider føles ekstra lange for Angela Fago. Hun er født i det sydlige Italien, i byen Taranto som ligger lige hvor støvlelandets hæl stikker ud fra skoen. Her bliver det sjældent rigtig koldt, fortæller hun.
»Jeg savner indimellem det varme klima. Sommernætterne hvor man aldrig behøver at tage en jakke på – og maden naturligvis«.
At hun skulle ende i Danmark, er ikke helt så tilfældigt, som det lyder. Hendes mor er nemlig dansk, mødte hendes far i Italien og flyttede siden til Syditalien, hvor de stadig bor.
»Da jeg blev færdig på universitetet i Parma, blev jeg ansat i Napoli, hvor jeg blandt andet undersøgte, hvordan antarktiske fisk kan klare sig i et miljø med en konstant temperatur under frysepunktet. Det var her, jeg blev interesseret i sammenhængen mellem oxygen og væv,« siger hun.
I 1993 rejste hun til Danmark, hvor hun fik en midlertidig forskerstilling på Aarhus Universitet. Det stod dog hurtigt klart for hende, at hun ikke ville rejse tilbage til Italien.
»Jeg elskede det her. I Danmark var det muligt at søge fondsmidler, selvom man er en ung forsker. Forskningen i zoofysiologi i Aarhus, som mine interesser hørte under, var desuden i verdensklasse. Så jeg blev, fik senere min egen forskningsgruppe og blev professor i 2015.«
Det første protein, der blev kortlagt
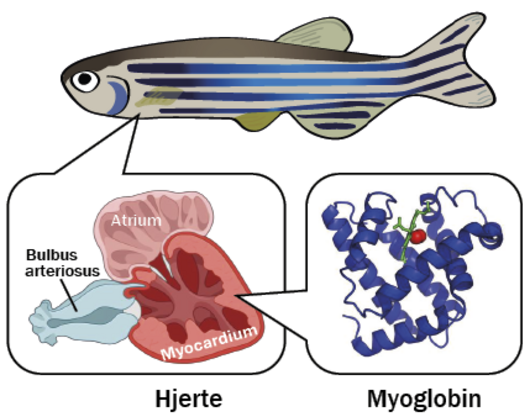
Myoglobin var det første protein, der blev kortlagt. Det skete i 1957, hvor det lykkedes John C. Kendrew at fastslå den tredimensionelle struktur af myoglobin ved hjælp af røntgenkrystallografi. Noget han sammen med Max Perutz fik nobelprisen for i 1962.
Myoglobin er i familie med det mere kendte protein hæmoglobin, som bærer oxygen i vores røde blodceller. Myoglobin blev kortlagt først, fordi det er markant mindre end hæmoglobin og derfor er enklere at kortlægge.
Begge proteiner udmærker sig ved at indeholde jern-atomer i reduceret tilstand (Fe2+), som binder oxygen til sig. Proteinerne kan holde på oxygenmolekylerne, og hæmoglobin bærer oxygen via blodet ud til cellerne i hele kroppen.
Fe2+ mangler to elektroner og søger derfor hele tiden efter molekyler med frie elektroner at binde sig til – og her er oxygen en af mulighederne. Dog ikke den eneste. Det er eksempelvis farligt at indånde for meget udstødning fra gamle biler, fordi den er fyldt med carbonmonoxid (CO), som binder sig til hæmoglobin og myoglobin i stedet for oxygen og dermed blokerer for oxygenoptagelsen.
Sådan ser reaktionen mellem jern og oxygen ud i myoglobin:
Mb(Fe2+) + O2 ↔ MbO2
hvor Mb(Fe2+) er deoxymyoglobin, O2 er oxygen og MbO2 er oxymyoglobin, hvor oxygenmolekylet har bundet sig til jernatomet.
En overraskende opdagelse
Overfor laboratoriet, på den anden side af en gang, som er fyldt med gamle arkivskabe og udstoppede dyr, ligger Angela Fagos kontor. På døren hænger forsider fra nogle af de videnskabelige publikationer, hendes forskning har været publiceret i. På reolen bag skrivebordet står ringbind og bøger i en sirlig orden.
Hun fortæller, at hun for alvor fik øjnene op for myoglobin, da flere forskningsgrupper rundt omkring i verden i slutningen af 1990’erne publicerede overraskende resultater. Ny genteknologi havde gjort det nemmere og billigere at deaktivere det gen, der bærer på opskriften på myoglobin i mus. Nu kunne man endelig med sikkerhed slå fast, hvilken rolle myoglobin spiller. Troede man.
Forskningsgrupperne regnede med, at de genredigerede mus ville blive små, svagelige og måske ikke nå voksenalderen, inden de døde. Men de tog fejl, forklarer Angela Fago.
»Nogle af musene døde, men langt de fleste overlevede. Det viste sig, at musene kunne klare sig med oxygen udelukkende fra blodomløbet. Nogle havde lidt større hjerter, men ellers var der ingen forskel fra de normale mus,« siger hun.
»Pludselig anede vi ikke, hvilken rolle proteinet spiller. Det var enormt spændende, og siden da har jeg været optaget af at løse mysteriet om, hvad myoglobin egentlig gør i dyr.«
Sammen med forskere fra Institut for Molekylærbiologi og Genetik på Aarhus Universitet og to ph.d.-studerende, Rasmus Hejlesen og Ciska Bakkeren, designede hun en række forsøg med zebrafisk, hvor myoglobin-genet var sat ud af spil. Hun håbede, at fiskene kunne give nogle klare svar.
»Vi valgte zebrafisk af flere grunde. De er billigere at have, de formerer sig i en fart og vokser lynhurtigt op. På den måde kan man komme gennem flere generationer og undersøge en række forskellige ting på nogle måneder.«

Bestemmelse af stofskifte
Figuren viser princippet i forskernes specialbyggede “vandløbebånd” – på fagsproget kaldet et svømmespirometer. Det måler en zebrafisks optag af oxygen ved hjælp af en lille sensor placeret i vandet, mens vandstrømmen kan bestemmes af en propel koblet til en motor. Fiskene tvinges til at svømme ved meget lav hastighed for at måle fiskens optag af oxygen under hvile (hvilestofskiftet) eller ved maksimal hastighed (målt i kropslængder per sekund) for at måle det maksimale stofskifte.
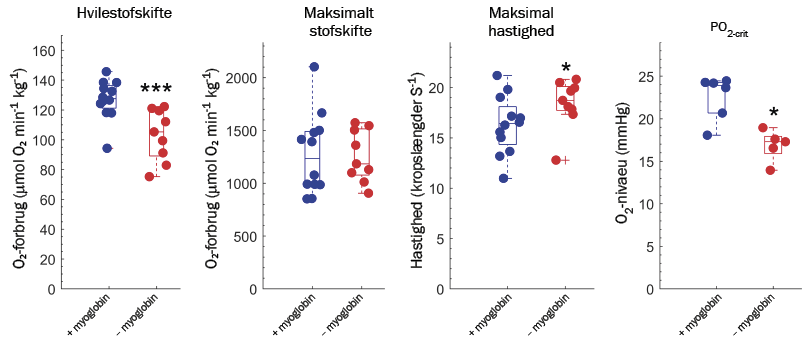
Graferne viser, at zebrafisk uden myoglobin-genet (data vist med rød) har et lavere oxygenforbrug under hvile, svømmer hurtigere, har samme maksimale oxygenforbrug (maksimal stofskifte) ved maksimal hastighed og tåler oxygenmangel bedre (lavere PO2crit) sammenlignet med ikke-genmodificerede zebrafisk (blå). PO2-crit angiver det oxygenniveau i vandet, hvor fisken ikke længere kan opretholde sit hvilestofskifte og derfor overgår til anaerobt energistofskifte, hvor energi produceres uden oxygen. Stjernerne over datapunkterne angiver i hvilken grad, der er signifikant forskel på de to grupper.
Troede at fiskene ville synke udmattede til bunds
En anden fordel ved zebrafiskene er, at man nemt kan tvinge dem til at svømme. En mus er derimod svær at tvinge op i hamsterhjulet, hvis den ikke vil.
»Vi designede vores fiskeløbebånd sådan, at fiskene er nødt til at svømme mod vandstrømmen. Hvis ikke, bliver de presset tilbage mod et plastikgitter,« siger Angela Fago.
Svømmespirometret gav professoren og hendes to ph.d.-studerende mulighed for at undersøge, hvad der sker med en zebrafisk uden myoglobin, når den bliver presset til det yderste. Noget, som ikke havde været muligt med musene.
»Vi troede, at fiskene hurtigt ville blive udmattede, når de manglede myoglobin. Men i kampen mod den stærke strøm, klarede de sig mindst lige så godt som de normale fisk. De sank ikke udmattede til bunds, men svømmede blot videre, og kunne endda svømme hurtigere. Det var ret vildt at se – og ganske overraskende. Nu ved vi med sikkerhed, at myoglobin ikke spiller en rolle i forhold til at sørge for ekstra oxygen til hjertet. I hvert fald ikke i zebrafisk, siger Angela Fago.
Sensoren i vandstrømmen kunne desuden måle, hvor meget oxygen fisken optog fra vandet, når den svømmede – og de genmodificerede fisk trak heller ikke mere oxygen ind i gællerne.
»Det blev vi meget overraskede over at se. Det betyder, at fiskene ikke engang behøver at kompensere ved at trække mere oxygen ind i blodet,« siger hun.
Spiller måske vigtig rolle i fosterstadiet
Hvis myoglobin ikke fungerer som en slags reservetank med ekstra oxygen, hvilken rolle har den så? Det er det helt store spørgsmål, som Angela Fago og hendes ph.d.-studerende Ciska Bakkeren nu prøver at besvare. Og de har en teori.
»Vi tror, at myoglobin spiller en vigtig rolle i den embryonale udvikling hos dyr og mennesker. Proteinet får muligvis de forskellige celler i hjerte- og muskelvæv til mere effektivt at differentiere sig til de celletyper, der er brug for, mens væv og organer bliver bygget,« siger ph.d.-studerende Ciska Bakkeren.
Det er svært at undersøge, hvad der præcist sker inde i embryonet. Heldigvis har voksne zebrafisk også evnen til at regenerere dele af dets hjerte. For at gøre det, er fisken dog nødt til at spole cellerne tilbage til et tidligere stadie, hvor de endnu ikke er specialiserede – ligesom de er i embryonet. Og det giver de to forskere en mulighed for at undersøge, om deres teori holder.
»Det er faktisk muligt at klippe en smule af zebrafiskens hjerte, sy fisken sammen igen og observere, hvad der sker,« forklarer Angela Fago og fortsætter:
»Vores tidligere ph.d.-studerende Rasmus Hejlesen – der nu er postdoc i Edinburgh – har under et forskerophold i USA fundet ud af, at de normale zebrafisk skruer ned for deres myoglobinproduktion, når de skal regenerere hjertevæv. Det tyder på, at cellerne dermed får mulighed for at spole tilbage. Når de begynder at specialisere sig igen, bliver der dog skruet op for myoglobinet.«
Når vi mennesker ikke kan regenerere dele af vores hjerte, skyldes det måske, at vi ikke kan skrue ned for myoglobinproduktionen på samme måde som zebrafisken.
»Noget tyder på, at myoglobin kommer med en pris. Det sørger for et velfungerende hjerte, der kan generere en masse energi, men du mister evnen til at regenerere det.
Måske kan vi udnytte de her mekanismer i zebrafisk til nye former for hjertebehandlinger af mennesker engang ude i fremtiden,« siger Angela Fago og slutter:
»Hvem ved. Måske kan vi omprogrammere vores celler til at regenerere hjertevæv, når vi bedre forstår, hvordan myoglobin virker.« ♦