
Kemi der bare klikker
For første gang i 25 år har en dansk forsker modtaget en Nobelpris. Kemikeren Morten Meldal får sammen med amerikanerne Barry Sharpless og Carolyn Bertozzi kemiprisen for deres bidrag til udviklingen af såkaldt klikkemi, der dækker over kunsten at bygge funktionelle molekyler ud fra simple byggesten.
Af Carsten R. Kjaer, Aktuel Naturvidenskab.
Midt i, at den samlede danske journaliststand var stimlet sammen for at stå klar til at fortælle om den ikke særlige overraskende nyhed, at der blev udskrevet valg – dukkede pludselig en anden kæmpenyhed op ud af det blå: En dansk kemiker havde modtaget Nobelprisen i Kemi! Det var professor Morten Meldal fra Københavns Universitet, der havde opnået den store ære, som han deler med de to amerikanske kemikere Barry Sharpless (som allerede har en nobelpris i Kemi i samlingen, nemlig fra 2001) og Carolyn Bertoz.
Sharpless og Meldal får deres del af prisen for at lægge grunden til såkaldt klikkemi, mens Bertozzi hædres for at udvikle klikkemien, så den kan anvendes i levende celler.
Svært at efterligne naturens molekyler
Begrebet “klikkemi” dækker over en tilgang, hvor man bygger funktionelle molekyler op ud fra simple byggeklodser. Barry Sharpless introducerede begrebet i en videnskabelig afhandling fra 2001. Heri argumenterede han for, at kemikerne i deres bestræbelser på at udvikle nye molekyler til brug i lægemidler burde gå væk fra at bestræbe sig på at efterligne naturlige molekyler, idet det alt for ofte leder til molekylære konstruktioner, der er meget vanskelige at styre. Hvis man finder et potentielt lægemiddel i naturen, er det ofte muligt at fremstille det i små mængder til test og kliniske forsøg. Men et kommercielt lægemiddel kræver, at stoffet kan fremstilles på industriel skala med høj effektivitet. Og det kan tage mange års arbejde at finde metoder til at opnå det.
En af de store udfordringer er bindingerne mellem carbonatomerne, som er vitale i al kemi i levende organismer. At få dem til at makke ret har vist sig notorisk vanskeligt. Årsagen er, at carbonatomer fra forskellige molekyler ofte mangler en kemisk drivkraft for at danne bindinger med hinanden, og derfor skal de kunstigt aktiveres. Men denne aktivering leder som oftest til talrige uønskede sidereaktioner, og derfor går en del af materialet tabt.

Kemi med simple byggeklodser
I stedet foreslog Sharpless i sin afhandling, at man starter med simple molekyler, som allerede har en komplet carbonstruktur. Disse molekyler kan så bindes sammen ved hjælp af nitrogen- og oxygenatomer, som er lettere at kontrollere. Ved at vælge simple reaktioner, hvor der naturligt er en stærk tendens til at molekylerne danner bindinger, kan man undgå mange uønskede sidereaktioner og dermed meget mindre spild.
Ved at kombinere simple kemiske byggeblokke kan man skabe et utal af molekyler, og Sharpless hævdede, at selvom klikkemi – som han kaldte tilgangen – ikke kan frembringe eksakte kopier af naturlige molekyler, vil det være muligt at finde molekyler, der grundlæggende har de samme funktioner. I sin publikation 2001 oplistede Sharpless en række kriterier for, hvad klikkemiske reaktioner skal leve op til, såsom at de skal kunne fungere under simple reaktionsbetingelser, give et højt udbytte og kun danne uskadelige biprodukter, som kan fjernes med simple metoder. Udgangsmaterialerne bør endvidere være let tilgængelige, og produktet bør være stabilt under fysiologiske forhold.
En tilfældig opdagelse
Med sin artikel fra 2001 satte Sharpless klikkemien på dagsordenen rent konceptuelt. Men den kemiske reaktion, som siden er blevet nærmest synonym med klikkemi, står den danske kemiker Morten Meldal bag. Reaktionen – kaldet kobberkatalyseret azidalkyn cycloaddition – opdagede han ved lidt af et tilfælde.
Omkring det tidspunkt, hvor Sharpless udgav sin artikel, arbejdede Morten Meldal med at udvikle metoder til at finde potentielle lægemidler. En dag skete der noget mærkeligt i forbindelse med et forsøg, der ellers burde være en ren rutineundersøgelse. Her forsøgte Meldal med sine kolleger at reagere en alkyn med en acylhalid – en reaktion, der plejede at forløbe ganske glat, blot man tilsatte kobberioner som katalysator. Men da Meldal undersøgte, hvad der var sket i reagensglasset denne dag, viste det sig, at alkynen havde reageret med den “forkerte” ende af acylhalid-molekylet. I den anden ende sad nu en kemisk gruppe kaldet en azid (N3-). Sammen med alkynen dannede azidet en ringformet struktur, en såkaldt triazol.
Triazoler er meget brugbare kemiske strukturer indenfor kemien. De er stabile og findes blandt andet i visse lægemidler, farvestoffer og agrokemiske produkter. Forskere havde derfor tidligere forsøgt at lave triazoler ud fra alkyner og azider, men det havde givet uønskede biprodukter. Meldal indså, at kobberionerne havde kontrolleret reaktionen, sådan at der i princippet kun blev dannet triazol.
Han præsenterede sin opdagelse ved et symposium i juni 2001 og senere i en videnskabelig artikel i 2002, hvor han viste, at reaktionen kunne anvendes til at binde mange forskellige molekyler sammen.
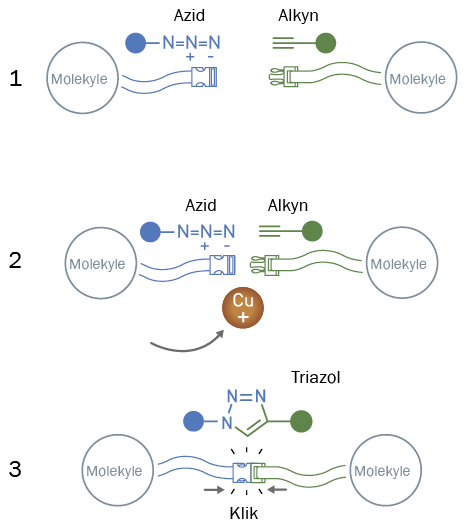
Den kobberkatalyserede reaktion mellem azider og alkyner har vist sig som den ideelle klik-reaktion. Azidet fungerer som en spændt fjeder, der udløses af kobberionen. Hvis en kemiker ønsker at forbinde to forskellige molekyler kan hun i dag relativt nemt introducere en azid på det ene molekyle og en alkyn på det andet og derefter klikke de to molekyler sammen ved at tilsætte kobberioner.
Enkeltheden i dette koncept har gjort reaktionen enormt populær i kemiske laboratorier verden rundt – både i grundforskningen og i private virksomheder.
Klikkemi i levende celler
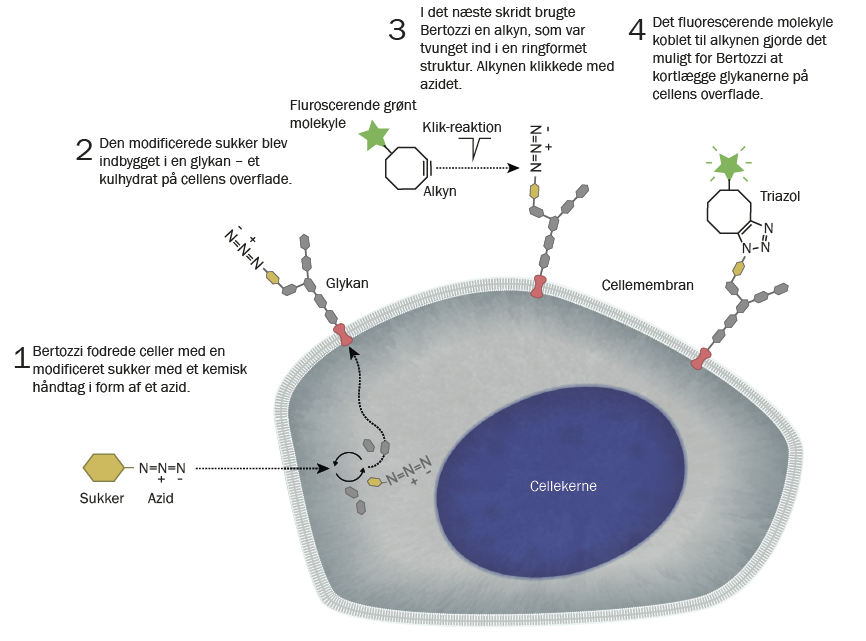
Den tredje af årets nobelpristagere, Carolyn Bertozzi, har populært sagt udviklet klikkemien, så den kan bruges i levende celler. Bertozzi studerede tilbage i 1990’erne glykaner, som er kulhydrater opbygget af forskellige sukkerstoffer, og som spiller en rolle i mange vigtige biologiske processer. Hun fandt en metode til at indbygge modificerede udgaver af sukkerstoffet sialinsyre i forskellige glykaner, hvor sialinsyre havde et kemisk håndtag. Dette håndtag kunne hun koble for eksempel et fluorescerende molekyle på, og på den måde kunne hun kortlægge, hvor glykanerne befandt sig i cellen – noget man ellers ikke kunne med eksisterende metoder. Hun fandt, at det optimale kemiske håndtag netop var et azid, fordi dette molekyle ikke påvirker cellen.
Da nyheden om Meldals kobberkatalyserede azidalkyn cycloaddition bredte sig, stod det klart for Bertozzi, at denne reaktion ville være yderst relevant at udnytte. Udfordringen var bare, at kobber er giftigt for levende organismer
Hun dykkede ned i litteraturen og opdagede, at azid og alkyn kan reagere nærmest eksplosivt med hinanden uden tilsætning af kobber, hvis alkynen er tvunget ind i en ringformet, kemisk struktur. Det viste sig at fungere fint, da hun testede det på levende celler, og i 2004 kunne hun publicere den modificerede udgave af reaktionen og vise, at den kunne bruges til at spore glykaner.
Siden har Bertozzi yderligere forfinet sin klikreaktion, så den virker endnu bedre i et cellemiljø, og hun og mange andre forskere har brugt disse reaktioner til at udforske, hvordan biomolekyler vekselvirker i celler og studere sygdomsprocesser. ♦