Den lange vej mod det absolutte nul
Vand koger ikke altid ved 100 grader. Jagten på et stabilt mål for varme førte fra 1700-tallets eksperimenter til kelvin – den absolutte skala for temperatur.
Af Kristian Hvidtfelt Nielsen
Der var engang, hvor selv det at koge vand kunne være et stort videnskabeligt problem. I slutningen af 1700-tallet forsøgte fysikere over hele Europa at finde et fast punkt på temperaturskalaen – et universelt udgangspunkt for at måle varme og kulde. Men vand viste sig at være et upålideligt referencepunkt. Det kogte ved én temperatur i bjergene, en anden i dalene, og endda forskelligt fra dag til dag i det samme laboratorium.
I 1776 nedsatte Royal Society i London et udvalg, ledet af Henry Cavendish, for at standardisere datidens termometre. Udvalget opdagede dog, at vands kogepunkt varierede med lufttrykket, og at de væsker, man målte varmen med i termometrenes glasrør, ikke havde samme varme overalt.
Det betød, at det i praksis var umuligt at lave entydige temperaturmålinger. Alligevel blev dette tidlige forsøg på jagt på at bruge vands kogepunkt som et fikspunkt på temperaturskalaen begyndelsen på den lange historie, der førte frem til den moderne temperaturmåling – og til den SI-enhed, vi i dag kalder kelvin.
Blod, smør og kogende vand
De første termometre med termometriske væsker som kviksølv, sprit og luft dukkede op allerede omkring år 1600. Galileo Galilei og hans samtidige lavede primitive “thermoskoper”, som blot viste, at luften udvidede sig, når det blev varmt. I løbet af 1600-tallet blev termometre taget i brug til mere videnskabelige målinger – men der var et problem: Ingen vidste, hvad tallene på skalaen betød.
Hver fabrikant havde sit eget system. Edmond Halley, bedst kendt for sin komet, beklagede sig i 1693 over, at “ingen termometre nogensinde viser det samme”. Nogle brugte den koldeste vinterdag eller den varmeste sommerdag som referencepunkt, mens Isaac Newton valgte kropsvarmen, og andre igen kogepunktet for vin. Den franske fysiker Joachim Dalencé foreslog endda at bruge smørs smeltepunkt som en øvre temperaturgrænse.
Det var først i begyndelsen af 1700-tallet, at vands fryse- og kogepunkt begyndte at blive bredt accepteret som et fælles fikspunkt. Vand var tilgængeligt overalt og virkede som en “naturlig” reference. Men som Cavendish og hans kolleger i Royal Society-udvalget snart opdagede, var naturen mindre stabil, end man havde håbet.
Den omvendte Celsius-skala
I 1742 foreslog den svenske astronom Anders Celsius en temperaturskala med to faste punkter: Vandets kogepunkt ved 0 grader og frysepunkt ved 100 grader, altså det omvendte af, hvad vi kender i dag. Celsius’ skala var centigrad, altså opdelt i 100 lige store grader.
Da Celsius døde året efter, valgte kollegerne i Uppsala – sandsynligvis Daniel Ekström eller Carl Linné – at vende hans skala om. Nu stod 0 grader for vands frysepunkt, og 100 grader for kogepunktet. Den omvendte skala passede bedre til den intuitive fornemmelse af, at varmen “stiger”.
At Celsius oprindeligt valgte den modsatte retning på sin skala, er dog ikke så mærkeligt. I 1700-tallet talte man stadig om “kuldegrader” som en selvstændig størrelse, på linje med varme. Nogle fysikere mente endda, at kulde var en substans – en slags kulde- eller “frigorisk” væske, der flød ud af kroppen, når temperaturen faldt. Først i løbet af 1800-tallet blev denne idé endegyldigt forladt til fordel for teorien om varme som bevægelse.
Uanset retningen var Celsius’ skala et vigtigt skridt mod standardisering af temperaturmåling. Den var enkel, præcis og tilgængelig, men den var også knyttet til vands og andre væskers fysiske egenskaber, som varierer med tryk og temperatur. Det var det, som voldte Royal Society-udvalget hovedbrud i slutningen af 1700-tallet.
Fahrenheit grundlægger en anden tradition
Omtrent samtidigt som Celsius udviklede Daniel Gabriel Fahrenheit i Amsterdam sit eget kviksølvtermometer. Han indførte en skala, hvor 32° svarede til isvand, og 212° til kogende vand. Fahrenheit valgte dette interval for at undgå negative tal og for at have en højere opløsning på sin temperaturskala.
Hans termometre var mere stabile end de tidligere termometre, der brugte sprit som termometrisk væske. De blev derfor hurtigt populære blandt læger og apotekere, der ville måle patienternes kropstemperatur eller temperaturen ved fremstilling af lægemidler med en hidtil uset nøjagtighed. Fahrenheit-skalaen blev standard i Storbritannien og senere i USA – et eksempel på, hvordan videnskabelige standarder ofte følger handel, sprog og kultur og ikke kun er udtryk for universelle naturkonstanter.
Temperatur og termodynamikken
I 1800-tallet gennemførte den franske fysiker Henri Victor Regnault omfattende målinger med kviksølv-, sprit- og lufttermometre for at finde en mere stabil sammenhæng mellem temperatur og volumenudvidelse. Regnaults metodiske arbejde afslørede, at ingen fysisk substans udvider sig fuldstændig ensartet med varmen. Det blev mere og mere uholdbart at bruge vand som fikspunkt.
William Thomson, bedre kendt som Lord Kelvin, blev den, der skabte et teoretisk fundament for temperaturbegrebet og -målinger. Inspireret af Sadi Carnots og James Joules tidlige arbejde indenfor termodynamik (læren om varmens bevægelse) definerede Kelvin i 1848 en absolut temperaturskala. Han ønskede, at den skulle være uafhængig af måleinstrument og gælde universelt for alle materialer.
I stedet for at tage udgangspunkt i vand, valgte Kelvin at betragte et legemes temperatur ud fra dets evne til at afgive varme og dermed udføre arbejde. Inspirationen kom særligt fra Carnots ide om den ideelle varmemaskine, hvor varme strømmer fra et varmt til et koldt legeme og undervejs kan omsættes til mekanisk arbejde.
I en sådan ideel proces afhænger mængden af det arbejde, der udføres, kun af forskellen mellem de to temperaturer – ikke af de materialer, der indgår i processen. Kelvin definerede forholdet mellem to temperaturer som forholdet mellem den varmeenergi, der optages fra det varme legeme, og den, der afgives til det kolde, når varme omdannes til arbejde i en Carnot-maskine.
Det absolutte nulpunkt
Med denne definition fik temperatur en teoretisk definition knyttet til begrebet energi frem for den empiriske måling af vandets kogepunkt. Den førte Kelvin videre til tanken om et absolut nulpunkt – den lavest mulige temperatur, hvor al varmebevægelse ophører, og intet arbejde længere kan udføres. Dette punkt, −273,15 °C, blev nulpunkt for den nye temperaturskala.
Kelvin ændrede dog ikke størrelsen på graderne, kun nulpunktet. Han beholdt Celsius’ inddeling, fordi den allerede var praktisk, velkendt og let at omsætte til eksperimentelle målinger. På den måde kunne forskere og ingeniører fortsætte med at bruge de samme temperaturforskelle som før – blot målt fra et nyt, absolut udgangspunkt.

Fra CGS til SI
Kelvin var ikke blot teoretiker, men også organisator. Han arbejdede for at skabe et system af ensartede enheder – det såkaldte CGS-system (centimeter, gram, sekund). Dette dannede senere grundlaget for det internationale metriske system, som blev formaliseret med Meterkonventionen i 1875.
Efterhånden som flere lande tilsluttede sig, blev ideen om fælles standarder et symbol på oplysningstidens idealer: præcision, rationalitet og internationalt samarbejde. Standardisering er dog ikke kun videnskab, men også politik. Lande som Storbritannien og USA var tilbageholdende med at acceptere SI-systemet, fordi de ikke så nogen praktisk gevinst i at skifte.
Samtidig var der et kulturelt og sprogligt aspekt: SI-enhederne blev forbundet med kontinentaleuropæiske idealer og særligt en udpræget fransk form for abstraktion og matematisk idealisering, mens de engelske mål (for eksempel inch, pound, gallon, Fahrenheit) blev set som mere anvendelige og almindelige, fordi de allerede var etableret som tekniske standarder indenfor håndværk og industri.
Kritikken mod fransk abstraktion kan måske virke underlig, hvad angår temperaturmåling. Det var jo skotten Lord Kelvin, der først havde foreslået den teoretisk funderede og universelle temperaturskala, og han var lige så empirisk og praktisk anlagt som andre britiske naturvidenskabsmænd. Men sådan var det – og er det til dels stadig, for USA har stadig ikke fuldt implementeret SI-systemet.
I SI-systemet fik Kelvin sin helt egen plads. Temperaturskalaen hedder nemlig kelvin (K), og i 1954 blev den fastlagt som 1/273,16 af vandets tredobbelte punkt – den tilstand, hvor is, vand og damp eksisterer i ligevægt ved præcis 0,01 °C.
Den nyeste definition
I 2019 blev SI-systemet omlagt, denne gang ud fra naturens mest fundamentale konstanter. Meteren blev knyttet til lysets hastighed, kilogrammet til Plancks konstant, sekundet til atomernes svingninger.
Kelvin-enheden blev defineret ud fra Boltzmanns konstant (k = 1,38×10⁻²³ J/K) – en størrelse, der forbinder energien i enkeltpartikler med den makroskopiske temperatur. Dermed forblev kelvin uafhængig af ethvert fysisk materiale, men stadig forankret i materiens mikroskopiske bevægelser.
Da Kelvin i 1848 offentliggjorde sin første artikel om en absolut temperaturskala, skrev han beskedent, at hans system kun var tænkt som et forslag til praktiske formål. Han kunne næppe have forudset, at hans navn en dag skulle være kendt som en af naturvidenskabens mest fundamentale enheder.
Måske ville det have glædet ham, at målet stadig er det samme som i 1700-tallet: At finde orden midt i naturens mangfoldighed og evige forandring. For selv om vand stadig nægter at koge ved den samme temperatur uafhængigt af omgivelserne, har vi lært at gøre denne uorden til grundlaget for en af de mest præcise måleenheder, mennesket nogensinde har skabt. ♦
Det absolutte nulpunkt og kvantefysik
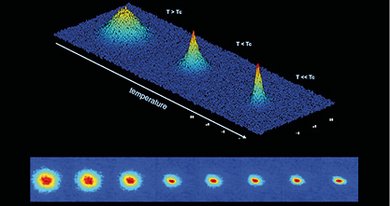
Det absolutte nulpunkt (0 K eller –273,15 °C) er den teoretiske grænse, hvor al termisk bevægelse ophører. Ifølge kvantefysikken kan atomer dog aldrig stå helt stille – de har altid en lille nulpunktenergi, som skyldes Heisenbergs usikkerhedsprincip.
Ved temperaturer tæt på nulpunktet begynder stof at opføre sig kvantemekanisk: Atomer kan smelte sammen i én fælles bølgefunktion og danne Bose–Einstein-kondensater, hvor materien mister sine klassiske egenskaber. De koldeste laboratorier på Jorden når i dag ned til få milliardtedele af en kelvin over nulpunktet – så tæt på absolut nul, som det bedste eksperimentelle udstyr i dag tillader.